Tổng số phụ: 150,000₫
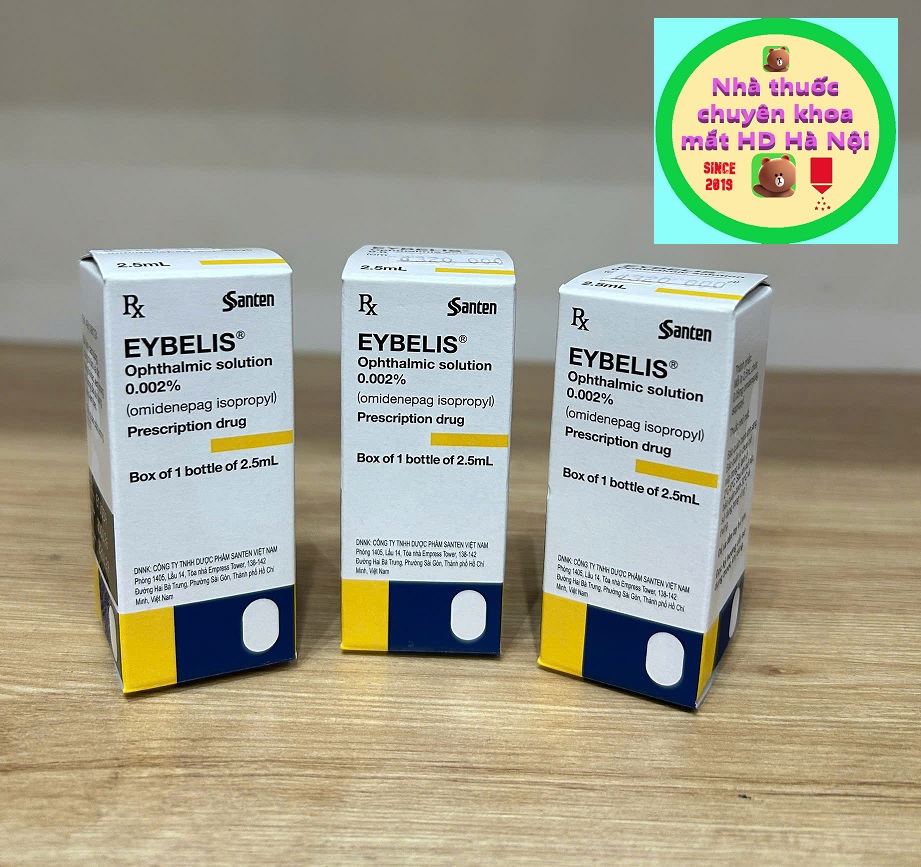
Eybelis 2.5ml
320,000₫
Eybelis là dung dịch nhỏ mắt chứa omidenepag isopropyl 0.002% – chất chủ vận chọn lọc thụ thể EP2. Số đăng ký thuốc: 499110981724
Rx – Thuốc kê đơn
A. Thành phần
- Hoạt chất: mỗi lọ Eybelis 2.5ml chứa 0.05 mg omidenepag isopropyl (0.002%)
- Tá dược: polyoxyl 35 castor oil, glycerin đậm đặc, dinatri edetat hydrat, natri citrat hydrat, acid citric hydrat, acid hydrocloric loãng, natri hydroxyd và nước tinh khiết.
- Chất bảo quản: benzalkonium clorid 0.005%
B. Dạng bào chế:
- Dung dịch nhỏ mắt Eybelis là dung dịch nhỏ mắt thân nước, trong, không màu, vô khuẩn.
- Dung dịch có pH 5.5-6.1 và áp lực thẩm thấu 0.9-1.1.
C. Chỉ định
- Glaucoma
- Tăng nhãn áp
D. Liều dùng và cách dùng
- Thuốc nhỏ mắt
- Nhỏ 1 giọt Eybelis vào mắt bị bệnh 1 lần mỗi ngày.
- Xử lý thuốc sau khi sử dụng: không có yêu cầu đặc biệt về xử lý thuốc sau khi sử dụng.
E. Chống chỉ định:
- Bệnh nhân có tiền sử quá mẫn với bất kỳ thành phần nào của thuốc Eybelis
- Bệnh nhân không có thủy tinh thể hoặc có thủy tinh thể nhân tạo [Eybelis có thể gây phù hoàng điểm kể cả phù hoàng điểm dạng nang đi kèm với tầm nhìn kém đi và suy giảm thị lực]. [Xem mục TÁC DỤNG KHÔNG MONG MUỐN]
F. Cảnh báo và thận trọng khi dùng thuốc Eybelis
F.1 Thận trọng quan trọng:
- Có thể xảy ra phù hoàng điểm kể cả phù hoàng điểm dạng nay hay viêm mống mắt. Hướng dẫn bệnh nhân tham vấn ngay với nhân viên y tế nếu gặp các bất thường như tầm nhìn kém đi. [Xem mục TÁC DỤNG KHÔNG MONG MUỐN]
F.2 Thận trọng liên quan đến các đối tượng bệnh nhân đặc biệt
- Bệnh nhân bị viêm mắt như viêm mống mắt và viêm màng bồ đào: viêm mắt có thể nặng hơn.
- Bệnh nhân Glaucoma góc đóng: chưa có kinh nghiệm lâm sàng.
- Sử dụng trên bệnh nhi: chưa có thử nghiệm lâm sàng nào đã được thực hiện trên trẻ em.
F.3 Thận trọng liên quan đến việc dùng thuốc
Bệnh nhân nên được hướng dẫn như sau:
- Cẩn thận không để đầu lọ thuốc chạm trực tiếp vào mắt để tránh nhiễm bẩn thuốc.
- Mở mắt bị bệnh và nhỏ thuốc vào túi kết mạc. Nhắm mắt trong 1-5 phút và ấn vào túi lệ, sau đó mở mắt ra.
- Nếu sử dụng nhiều hơn một loại thuốc tra mắt, nên dùng cách nhau ít nhất 5 phút.
- Sản phẩm nên được đặt ở nơi tránh ánh sáng.
- Thuốc này chứa 0.05 mg Benzalkonium clorid trong mỗi ml dung dịch tương đương với 0.125mg benzalkonium clorid trong mỗi lọ 2.5ml
- Benzalkonium clorid có thể bị hấp thu bởi kính áp tròng mềm và có thể làm thay đổi màu sắc của kính áp tròng. Nên tháo kính áp tròng trước khi sử dụng thuốc này và đeo lại sau khi sử dụng thuốc 15 phút.
- Benzalkonium clorid cũng có thể gây ra kích ứng mắt, đặc biệt nếu bệnh nhân bị khô mắt hoặc rối loạn giác mạc (lớp trong suốt ở phía trước của mắt). Nếu bệnh nhân cảm thấy có bất thường ở mắt, cay mắt hoặc đau trong mắt sau khi sử dụng thuốc, xin hãy thông báo với bác sĩ.
G. Sử dụng thuốc cho phụ nữ có thai và cho con bú
G.1 Phụ nữ có thai
- Chỉ sử dụng Eybelis cho phụ nữ có thai hoặc có khả năng mang thai nếu lợi ích điều trị mong đợi hơn hẳn các nguy cơ có thể xảy ra do dùng thuốc. Khi omidenepag isoproyl được tiêm dưới da cho thỏ mang thai với liều 0.8 mg/kg/ngày (gấp 40.000 lần liều dùng trên lâm sàng*), đã quan sát thấy tăng chết phôi/ chết thai và giảm tỷ lệ chết sau khi làm tổ, trong khi số lượng thai sống và khả năng sống sót của thai nhi giảm.
- * Liều dùng trên lâm sàng của omidenepag isopropyl (0.02 µg/kg/ngày): khi một giọt (30 µL) của sản phẩm này (omidenepag isopropyl 0.002%) được nhỏ cùng lúc vào cả hai mắt của một bệnh nhân cân nặng 60 kg.
G.2 Phụ nữ cho con bú
- Khi dùng Eybelis cho phụ nữ đang cho con bú, nên cân nhắc việc cho con bú dựa trên lợi ích của việc cho trẻ bú mẹ và lợi ích của việc điều trị. Trong một lần tiêm dưới da 0.03 mg/kg omidenepag isopropyl được đánh dấu 14C cho chuột trong thời kỳ cho con bú, chất này không được phát hiện trong sữa của chuột, tuy nhiên, chưa rõ omidenepag isopropyl có được bài tiết vào sữa mẹ hay không.
H. Ảnh hưởng lên khả năng lái xe và vận hành máy móc
- Do nhìn mờ tạm thời hoặc nhạy cảm với ánh sáng có thể xảy ra sau khi nhỏ Eybelis, hướng dẫn bệnh nhân không lái xe hoặc vận hành máy móc cho đến khi các triệu chứng này mất đi.
I. Tương tác thuốc và tương kỵ
I.1 Tương tác thuốc
- Chống chỉ định dùng đồng thời (không dùng đồng thời các thuốc sau)
| Thuốc | Các dấu hiệu, triệu chứng và cách điều trị | Cơ chế/ Các yếu tố nguy cơ |
| Dung dịch nhỏ mắt Tafluprost
Dung dịch nhỏ mắt phối hợp có chứa Tafluprost |
Nhạy cảm với ánh sáng mức độ vừa đến nặng và viêm mắt như viêm mống mắt thường được quan sát thấy | Chưa rõ cơ chế |
- Thận trọng khi dùng đồng thời (nên thận trọng khi dùng đồng thời thuốc này với các thuốc sau).
| Thuốc | Các dấu hiệu, triệu chứng và cách điều trị | Cơ chế/ Các yếu tố nguy cơ |
| Các thuốc điều trị Glaucoma / tăng nhãn áp (như timolol maleat) ngoại trừ tafluprost | Tần suất gặp tác dụng không mong muốn viêm mắt kể cả sung huyết kế mạc tăng lên khi dùng đồng thời với timolol maleat.
Chưa có kinh nghiệm dùng đồng thời với các loại thuốc khác |
Chưa rõ cơ chế |
I.2 Tương kỵ
- Do không có các nghiên cứu về tính tương kỵ của thuốc, không trộn lẫn thuốc này với các thuốc khác.
J. Tác dụng không mong muốn
- Do các tác dụng không mong muốn sau đây có thể xảy ra, nên theo dõi bệnh nhân chặt chẽ. Nếu quan sát thấy bất thường, nên thực hiện các biện pháp thích hợp như ngừng dùng thuốc.
Các tác dụng không mong muốn có ý nghĩa về mặt lâm sàng:
J.1 Phù hoàng điểm kể cả phù hoàng điểm dạng nang (5.2%)**
Nếu phát hiện các triệu chứng như suy giảm thị lực hoặc tầm nhìn kém đi, nên kiểm tra thị lực và soi chi tiết đáy mắt ngay lập tức. Nên cân nhắc làm thêm xét nghiệm chụp cắt lớp quang học (OCT) hoặc chụp mạch huỳnh quang đáy mắt nếu có sẵn. Nếu thấy phù hoàng điểm, cần tiến hành các biện pháp thích hợp như ngưng dùng thuốc. [Xem mục CHỐNG CHỈ ĐỊNH và CẢNH BÁO và THẬN TRỌNG KHI DÙNG THUỐC].
** Tất cả các biến cố bất lợi nêu trên đều được thấy ở những bệnh nhân có thủy tinh thể nhân tạo.
J.2 Các tác dụng không mong muốn khác.
| Cơ quan/ Tỉ lệ mắc | ≥ 10% | Từ 1% đến < 10% | Chưa rõ tỉ lệ mắc |
| Rối loạn về mắt | Sung huyết kết mạc (22.8%) | Dày giác mạc, viêm mống mắt (có tế bào trong tiền phòng, có protein trong tiền phòng), đau mắt, nhạy cảm ánh sáng, khó chịu ở mắt (như kích ứng mắt) và các rối loạn biểu mô giác mạc | Cảm giác khô mắt |
| Rối loạn hệ thần kinh | Đau đầu |
Thông báo ngay cho bác sỹ hoặc dược sỹ những phản ứng có hại gặp phải khi sử dụng thuốc.
K. Quá liều và xử trí
- Không có dữ liệu về sử dụng thuốc quá liều, không dùng quá liều chỉ định của thuốc.
- Bệnh nhân cần được tích cực theo dõi để có biện pháp xử trí kịp thời.
L. Đặc tính dược lực học
- Nhóm dược lý: các giác quan – nhãn khoa – các chế phẩm điều trị Glaucoma và co đồng tử – Các chế phẩm điều trị glaucoma khác
- Mã ATC: S01EX06
L.1 Cơ chế tác dụng:
- Cơ chế tác dụng làm giảm áp lực nội nhãn (IOP) của dung dịch nhỏ mắt omidenepag isopropyl được cho là làm tăng thoát thủy dịch qua con đường vùng bè và con đường màng bồ đào củng mạc bằng việc kích thích thụ thể EP2 (E-prostanoid subtype 2)
- Ái lực với các thụ thể prostanoid: omidenepag (chất chuyển hóa có hoạt tính) gắn chọn lọc với thụ thể EP2 (Ki =3.6 nM), và cho thấy hoạt tính chủ vận hiệu lực mạnh với thụ thể EP2 (EC50 = 8.3 nM). (in vitro)
- Động lực học thủy dịch: động lực học thủy dịch ở khỉ bị tăng nhãn áp do tia laser đã được xác định bằng cách sử dụng phương pháp fluorophotometry khi nhỏ dung dịch nhỏ mắt omidenepag isopropyl 0.002% vào mắt khỉ 1 lần mỗi ngày trong bảy ngày: không quan sát thấy thay đổi trong việc sản xuất thủy dịch trong khi có sự tăng rõ rệt việc thoát thủy dịch (được cho là qua con đường vùng bè) và qua màng bồ đào củng mạc.
L.2 Tác dụng làm hạ áp lực nội nhãn (IOP)
- Khi dung dịch nhỏ mắt omidenepag isoproyl ở các nồng độ khoảng từ 0.0001% đến 0.01% được nhỏ 1 lần mỗi ngày trong bảy ngày vào mắt của những con khỉ có nhãn áp bình thường, đã quan sát thấy tác dụng hạ nhãn áp IOP theo cách thức phụ thuốc liều và duy trì không giảm tác dụng từ ngày thứ nhất đến ngày thứ 7.
- Đã quan sát thấy tác dụng hạ IOP đáng kể khi nhỏ liều đơn dung dịch nhỏ mắt omidenepag isopropyl 0.01% cho khỉ bị tăng nhãn áp do tia laser.
L.3 Các thử nghiệm lâm sàng về an toàn và hiệu quả
Các thử nghiệm pha II/ III tại Nhật Bản
- Một thử nghiệm lâm sàng nhóm song song, được làm mù nghiên cứu viên, sử dụng thuốc này (1 lần mỗi ngày) và thuốc đối chứng (dung dịch nhỏ mắt latanoprost 0.005%, 1 lần mỗi ngày) đã được tiến hành trên 190 bệnh nhân bị tăng nhãn áp hoặc Glaucoma góc mở nguyên phát (189 đối tượng trong nhóm phân tích dữ liệu toàn bộ). Tác dụng hạ áp lực nội nhãn (IOP) được quan sát thấy kể từ lần thăm khám đầu tiên theo kế hoạch (Tuần 1) trở đi. Các kết quả cho thấy sự thay đổi áp lực nội nhãn (Trung bình ± SD) của Eybelis là -5.96 ± 2.45 mmHg ở tuần 4, kết quả này xác nhận sản phẩm không thua kém so với thuốc đối chứng.
- Tỷ lệ các đối tượng có ADR trong đợt điều trị là 39.4% (37/94 đối tượng). ADR thường được ghi nhận là sung huyết kết mạc (24.5% (23/94 đối tượng).
Bảng so sánh áp lực nội nhãn (IOP) mmHG trong nghiên cứu pha II / III
| Eybelis (Omidenepag isopropyl 0.002%)
(N = 94) |
Thuốc đối chứng (Latanoprost 0.005%)
(N = 95) |
|
| IOP trong ngày trung bình ở thời điểm ban đầu | 23.78 ± 1.73 | 23.40 ± 1.51 |
| IOP trong ngày trung bình tại tuần 4 | 17.81 ± 2.41 | 16.96 ± 2.24 |
| Thay đổi IOP trong ngày trung bình tại tuần 4 so với IOP ở thời điểm ban đầu | -5.96 ± 2.45 | -6.45 ± 2.01 |
| Sự khác biệt IOP trong ngày trung bình tại tuần 4 giữa các nhóm dùng thuốc (giá trị của nhóm dùng sản phẩm – giá trị của nhóm dùng thuốc đối chứng) | 0.63 | |
| Khoảng tin cậy 95% giữa các nhóm | 0.01 – 1.26 | |
(Trung bình ± SD)
M. Đặc tính dược động học
M1. Nồng độ trong máu
- Các nồng độ trong huyết tương của omidenepag (chất chuyển hóa có hoạt tính) đã được xác định khi nhỏ dung dịch nhỏ mắt omidenepag isopropyl 0.0025% *** vào cả 2 mắt của 14 người tình nguyện trưởng thành, khỏe mạnh (bảy người Nhật Bản và bảy người da trắng) 1 giọt mỗi lần, ngày 1 lần trong bảy ngày.
- Ở ngày 1, nồng độ đỉnh ở các đối tượng người Nhật Bản đạt 41.5 pg/ml sau khi nhỏ thuốc khoảng 9 phút trong khi nồng độ đỉnh ở các đối tượng người da trắng là 27.2 pg/ml sau khi nhỏ thuốc khoảng 10 phút. Ở ngày 7, nồng độ đỉnh ở các đối tượng người Nhật Bản đạt 37.5 pg/ml sau khi dùng khoảng 12 phút và ở các đối tượng người da trắng là 33.3 pg/ml sau khi nhỏ thuốc khoảng 11 phút, tương ứng. Thời gian bán thải là 23 ~ 32 phút.
M.2 Phân bố
- Nồng độ trong các mô mắt đạt đỉnh trong khoảng 15 phút đến 4 giờ sau khi nhỏ liều đơn dung dịch nhỏ mắt 14C-omidenepag isopropyl 0.03% *** vào mắt khỉ. Nồng độ cao đã được quan sát thấy đặc biệt ở giác mạc, kết mạc và vùng bè. Trong các mô này, nồng độ đạt đỉnh sau khi nhỏ thuốc 15 phút, và 14C-omidenepag isopropyl được thải trừ sau đó.
M.3 Chuyển hóa
- CYP3A4 tham gia vào quá trình chuyển hóa omidenepag ở người (in vitro).
- Omidenepag isopropyl được cho là bị thủy phân bởi các esterase thành dạng có hoạt tính dược lý, omidenepag, và cũng được chuyển hóa bằng khử N-alkyl. Omidenepag được cho là tiếp tục bị chuyển hóa bằng quá trình oxy hóa, khử N-alkyl, glucuronid hóa, liên hợp sulfat hoặc liên hợp taurine.
- *** nồng độ của thuốc là 0.002%
N. Quy cách đóng gói
- Hộp 1 lọ 2.5ml
O. Bảo quản
- Bảo quản tránh ánh sáng
- Bảo quản lọ chưa mở nắp trong tủ lạnh ở 2 – 8 độ C. Sau khi mở nắp, bảo quản dưới 30 độ C và sử dụng trong vòng 1 tháng.
P. Hạn dùng
- 36 tháng kể từ ngày sản xuất
Q. Tiêu chuẩn chất lượng
- Tiêu chuẩn cơ sở
R. Cơ sở sản xuất
SANTEN PHARMACEUTICAL CO.,LTD.
Sản xuất tại:
- Nhà máy Shiga: 348-3, Aza-suwa, Oaza-shide, Taga-cho, Inukami-gun, Shiga, Nhật Bản
Đóng gói và xuất xưởng lô tại:
- Nhà máy Noto: 2-14, Shikinami, Hodatsushimizu -cho, Hakui-gun, Ishikawa, Nhật Bản
Tham khảo các phẩm điều trị Glaucoma khác cùng Hãng Santen:
- Cosopt lọ 5ml: https://nhathuocmathdhanoi.com/product/cosopt-5ml/
- và Cosopt-S hộp 60 tép: https://nhathuocmathdhanoi.com/product/cosopt-s/

 Bronuck 0.1% 5ml - Nhật
Bronuck 0.1% 5ml - Nhật